Boraani, mikä tahansa boorin ja vedyn tai niiden johdannaisten epäorgaanisten yhdisteiden homologisesta sarjasta.
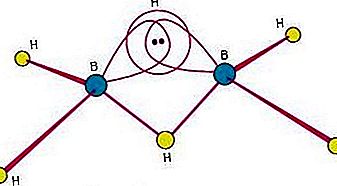
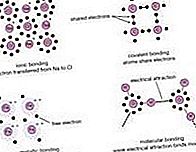
kemiallinen sidos: Boranes
Kuten aikaisemmin todettiin, elektronipuutosyhdistettä diboraania, B2H6, voidaan pitää yhdessä pidettyjen atomien ryhmänä
Boorihydridejä syntetisoitiin ensin systemaattisesti ja karakterisoitiin ajanjaksolla 1912 - suunnilleen vuoteen 1937 saksalainen kemisti Alfred Stock. Hän kutsui niitä boraaneiksi analogisesti alkaanien (tyydyttyneiden hiilivetyjen), hiilen hydridien (C) kanssa, joka on boorin naapuri jaksotaulukossa. Koska kevyemmät boraanit olivat haihtuvia, herkkiä ilmalle ja kosteudelle ja myrkyllisiä, Stock kehitti korkea-tyhjiömenetelmiä ja -laitteita niiden tutkimiseksi. Amerikkalainen boraanityö aloitettiin vuonna 1931 Hermann I. Schlesingerin ja Anton B. Burgin toimesta. Boranes pysyi ensisijaisesti akateemisen mielenkiinnon kohteena toiseen maailmansotaan saakka, jolloin Yhdysvaltojen hallitus tuki tutkimusta haihtuvien uraaniyhdisteiden (boorihydridien) löytämiseksi isotooppien erottamiseen, ja 1950-luvulle, jolloin se tuki korkea-energiapolttoaineiden kehittämisohjelmia raketteihin ja suihkukoneisiin. (Boraaneilla ja niiden johdannaisilla on paljon suurempi palamislämpö kuin hiilivetypolttoaineilla.) William Nunn Lipscomb, Jr, sai vuoden 1976 Nobelin kemian palkinnon "tutkimuksistaan boraanien rakenteesta, jotka valaisevat kemiallisen sitoutumisen ongelmia", kun taas yksi Schlesingerin opiskelijat, Herbert Charles Brown, jakoivat vuoden 1979 palkinnon hydroboraatioreaktiostaan (1956), joka on huomattavasti helppo lisätä BH: ta3 (muodossa BH 3 · S), jolloin tyydyttymättömien orgaanisten yhdisteiden (eli alkeenit ja alkyynit) eetteriliuottimissa (S) huoneenlämpötilassa saanto organoboraanit kvantitatiivisesti (eli reaktion, joka etenee kokonaan, tai lähes kokonaan, loppuun). Hydroboraatioreaktio puolestaan avasi uusia tutkimusreittejä stereospesifisen orgaanisen synteesin alalla.
Stock: n valmistamilla boraaneilla oli yleinen koostumus B n H n + 4 ja B n H n + 6, mutta tunnetaan monimutkaisempia lajeja, sekä neutraaleja että negatiivisia (anionisia). Boorin hydridejä on enemmän kuin minkä tahansa muun alkuaineen paitsi hiilen. Yksinkertaisin eristettävä boraani on B 2 H 6, diboraani (6). (Suluissa oleva arabialainen numero osoittaa vetyatomien määrän.) Se on yksi laajimmin tutkituista ja synteettisesti hyödyllisimmistä kemiallisista välituotteista. Se on kaupallisesti saatavissa, ja siitä valmistettiin vuosien ajan monia boraaneja ja niiden johdannaisia joko suoraan tai epäsuorasti. Vapaa BH 3 (ja B 3 H 7) ovat erittäin epävakaita, mutta ne voidaan eristää stabiilin adduktit (additiotuotteita) kanssa Lewis-emästen (elektroneja luovuttavan molekyylit) -eg, BH 3 -N (CH 3) 3. Boraanit voivat olla kiinteitä aineita, nesteitä tai kaasuja; yleensä niiden sulamis- ja kiehumispisteet kasvavat monimutkaisuuden ja molekyylipainon kasvaessa.
Boraanien rakenne ja kiinnitys
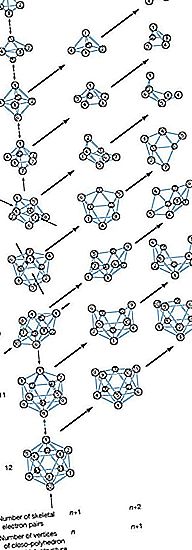
Sen sijaan, että esitettäisiin hiiliyhdisteiden yksinkertaisia ketju- ja rengaskonfiguraatioita, monimutkaisempien boraanien booriatomit sijaitsevat monihalkaiden kulmissa, joita voidaan pitää joko deltaderoneina (kolmiomaisilla pinnoilla olevilla monihalkaisimilla) tai deltaedrioksisilla katkelmilla. Näiden boori-klustereiden ymmärtämisen kehittäminen on auttanut kemistejä rationalisoimaan muiden epäorgaanisten, organometallisten ja siirtymämetalliklusteriyhdisteiden kemiaa.
Yhdessä useista nimikkeistöjärjestelmistä, joita Kansainvälisen puhtaan ja sovelletun kemian liitto (IUPAC) ehdottaa, on ominaisia rakenteellisia etuliitteitä: (1) klosos (latinalaisesta clovisista koostuvan ”klovon” korruptio, tarkoittaen ”häkki”), n booriatomit; (2) nido- (Latinalaisen nidus, tarkoittaa ”pesä”), nonclosed rakenteita, joissa B n klusterin sijaitsee n kulmat (n + 1) nurkkainen polyhedron-eli sellainen closo-polyhedron yksi puuttuu kärki; (3) arakno- (kreikkalainen, tarkoittaen "hämähäkinverkkoa"), vielä avoimempia klustereita, joissa booriatomit vievät (n + 2) kulmassa olevan monihalkaisijan n vierekkäisiä kulmia - ts. Suljettu monikerros, jossa on kaksi puuttuvaa kärkeä; (4) hypofysiikka (kreikkalainen, joka tarkoittaa ”kutomaan” tai “verkkoa”), avoimimpia klustereita, booriatomien ollessa (n + 3) kulmassa olevan kolo-monikerron n kulmassa; ja (5) klado- (kreikka, tarkoittaen ”haaraa”), n: n booriatomin käyttämän n + 4-kärkisen sulkemispolyedronin kärki. Hypofossi- ja klado-sarjojen jäsenet tunnetaan tällä hetkellä vain boraanijohdannaisina. Kahden tai useamman näiden moniradioraalisten boraaniklusterien välinen yhteys on merkitty etuliitteellä conjuncto- (latina, mikä tarkoittaa ”liittyä yhteen”). Esimerkiksi, conjuncto-B 10 H 16 on valmistettu liittämällä B 3 H 8 yksikköä kahdesta B 6 H 9 molekyylien kautta B-sidoksen.
Yksi syy boraaneihin liittyvään suureen kiinnostukseen on se, että niiden rakenteet eroavat muista luokkien yhdisteistä. Koska boraanien sitomiseen sisältyy monen keskuksen sitoutuminen, jossa kolme tai useampi atomi jakaa parin sidoselektroneja, boraaneja kutsutaan yleisesti elektronivajeiksi aineiksi. Diboraanilla (6) on seuraava rakenne:
Tähän rakenteeseen sisältyy kolmen keskuksen siltasidonta, jossa yksi elektronipari on jaettu kolmen (eikä kahden) atomin - kahden booriatomin ja yhden vetyatomin - kesken. (Katso kemiallinen sitoutuminen: Kemiallisen sitoutumisen edistyneet näkökohdat: Boraanit keskusteluun kolmen keskuksen sidoksesta.) Boorin kyky muodostaa sellaisia sidoksia normaalien kovalenttisten sidosten lisäksi johtaa monimutkaisten moniradioboraanien muodostumiseen.