Konformaatio, mikä tahansa äärettömästä määrästä mahdollisia atomien spatiaalisia järjestelyjä molekyylissä, joka johtuu sen muodostamien atomiryhmien pyörimisestä yksittäisten sidosten ympärille.
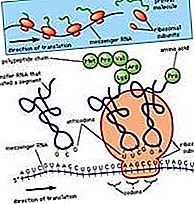
proteiini: Proteiinien konformaatio rajapinnoissa
Kuten monissa muissa aineissa, joissa on sekä hydrofiilisiä että hydrofobisia ryhmiä, liukoisilla proteiineilla on taipumus siirtyä ilman väliseen rajapintaan.
Erilaiset muodonmuutokset ovat mahdollisia jokaiselle molekyylille, jossa yksi kovalenttinen sidos yhdistää kaksi polyatomia ryhmää, joista jokaisessa ainakin yksi atomi ei ole kyseessä olevan yksittäisen sidoksen akselia pitkin. Yksinkertaisin tällainen molekyyli on vetyperoksidi, jossa kaksi hydroksyyliryhmää voivat pyöriä toistensa suhteen happi-happea-sidoksen akselin ympäri. Läsnä on enemmän kuin yksi tällainen yksinkertainen sidos molekyylissä-, kuten siitä, että propaania (CH 3 -CH 2 -CH 3), esimerkiksi, vain lisää monimutkaisuutta tilanteen muuttamatta sen luonnetta. Molekyyleissä, kuten syanogeenin (N≡C ― C≡N) tai butadiyreenin (H ― C≡C ― C≡C ― H), kaikki atomit sijaitsevat keski-yksisidoksen akselia pitkin, joten ei ole erotettavissa olevia muodonmuutoksia olla olemassa.
Yleensä jokainen erotettavissa oleva molekyylin konformaatio edustaa eri potentiaalienergian tilaa, koska houkuttelevat tai heijastavat voimat toimivat rakenteen eri osien välisen etäisyyden mukaan. Jos nämä voimat puuttuisivat, kaikilla konformaatioilla olisi sama energia ja pyöriminen yksittäisen sidoksen ympärillä olisi täysin vapaa tai rajoittamaton. Jos voimat ovat voimakkaita, erilaiset muodonmuutokset eroavat toisistaan suuresti energian tai stabiilisuuden suhteen: molekyyli vie tavallisesti vakaan tilan (yksi vähän energiaa kuluttavaan tilaan) ja siirtyy toiseen vakaaan tilaan vasta, kun se absorboi tarpeeksi energiaa saavuttaakseen ja kulkeakseen epävakaan väliintulon läpi. konformaatiossa.
Esimerkiksi metaanin sisäiset voimat etaanissa ovat niin heikkoja, että niiden olemassaolon voidaan päätellä vain hienoisista vaikutuksista termodynaamisiin ominaisuuksiin, kuten entalpiaan ja entropiaan. (Vaikka sisäistä kiertoa etaanissa rajoitettaisiin ankarasti, sen kolme vakainta konformaatiota eivät ole erotettavissa.) Tiettyjen monimutkaisempien yhdisteiden molekyylirakenteet kuitenkin asettavat niin voimakkaita kiertoesteitä, että stereoisomeeriset muodot - jotka eroavat vain konformaatiosta - ovat riittävän vakaita olla eristetty.





![Mitä ikinä tapahtui Baby Janelle? elokuva Aldrich [1962] Mitä ikinä tapahtui Baby Janelle? elokuva Aldrich [1962]](https://images.thetopknowledge.com/img/entertainment-pop-culture/2/what-ever-happened-baby-jane-film-aldrich-1962.jpg)