Fluori (F), reaktiivisin kemiallinen elementti ja halogeenielementtien kevyin jäsen, tai jaksollisen ryhmän 17 ryhmä VIIa. Sille kemiallisen aktiivisuuden voidaan katsoa johtuvan sen äärimmäisestä kyvystä houkutella elektroneja (se on kaikkein elektronegatiivisin elementti) ja sen atomien pieni koko.
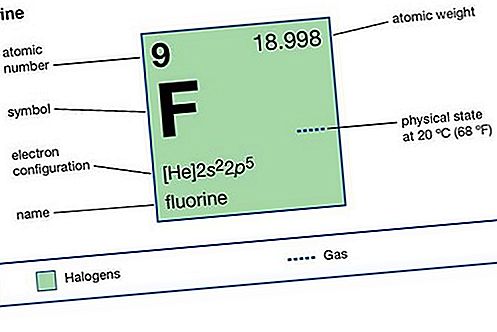
Elementin ominaisuudet
| atominumero | 9 |
|---|---|
| atomipaino | 18,9984 |
| sulamispiste | −219,62 ° C (−363,32 ° F) |
| kiehumispiste | −188 ° C (−306 ° F) |
| tiheys (1 atm, 0 ° C tai 32 ° F) | 1,696 g / litra (0,226 unssi / gallona) |
| hapetustilat | -1 |
| elektronikonfig. | 1s 2 2s 2 2p 5 |
Historia
Fluoripitoinen mineraalifluori (tai fluoriitti) kuvasi vuonna 1529 saksalainen lääkäri ja mineralogist Georgius Agricola. Vaikuttaa todennäköiseltä, että raakafluorivetyhappoa valmisti ensin tuntematon englantilainen lasinvalmistaja vuonna 1720. Vuonna 1771 ruotsalainen kemisti Carl Wilhelm Scheele sai fluorivetyhapon epäpuhtaassa tilassa kuumentamalla fluorilaastia väkevällä rikkihapolla lasiretortissa, jota syövytettiin voimakkaasti. tuote; seurauksena metallista valmistettuja astioita käytettiin myöhemmissä kokeissa aineen kanssa. Lähes vedettömä happo valmistettiin vuonna 1809, ja kaksi vuotta myöhemmin ranskalainen fyysikko André-Marie Ampère ehdotti, että se oli vetyyhdiste, jolla on tuntematon alkuaine, kloorin tapainen, jolle hän ehdotti nimeä fluori. Sitten fluorilaastin todettiin olevan kalsiumfluoridi.
Fluorin eristäminen oli pitkään yksi tärkeimmistä epäorgaanisen kemian ratkaisemattomista ongelmista, ja vasta vuonna 1886 ranskalainen kemisti Henri Moissan valmisti alkuaineen elektrolysoimalla kaliumvetyfluoridiliuosta vetyfluoridissa. Hän sai vuoden 1906 Nobelin kemian palkinnon fluorin eristämisestä. Alkuaineen käsittelyvaikeudet ja sen myrkylliset ominaisuudet myötävaikuttivat hitaaseen fluorikemian kehitykseen. Itse asiassa toisen maailmansodan aikaan elementti näytti olevan laboratorio-uteliaisuus. Sitten kuitenkin uraaniheksafluoridin käyttö uraani-isotooppien erottelussa yhdessä teollisuuden kannalta tärkeiden orgaanisten fluoriyhdisteiden kehittämisen kanssa teki fluorista huomattavan hyödyllisen teollisuuskemikaalin.
Esiintyminen ja jakauma
Fluoripitoista mineraalifluorisälöä (fluoriitti, CaF 2) on käytetty vuosisatojen ajan fluxina (puhdistusaineena) useissa metallurgisissa prosesseissa. Nimi fluorilasi on johdettu latinan kielestä, virtaamaan. Myöhemmin mineraali osoittautui alkuaineen lähteeksi, joka nimettiin vastaavasti fluoriksi. Värittömillä, läpinäkyvillä fluorilasi-kiteillä on sinertävä valaistus, ja tämä ominaisuus tunnetaan vastaavasti fluoresenssina.
Fluori esiintyy luonnossa vain sen kemiallisten yhdisteiden muodossa, lukuun ottamatta fluorisävyssä olevan vapaan alkuaineen pieniä määriä, joille on annettu säteilyn säteilyä. Ei harvinainen elementti, se muodostaa noin 0,065 prosenttia maankuoresta. Tärkeimmät fluoria sisältävät mineraalit ovat (1) fluorisälpä, jonka talletuksia esiintyy Illinoisissa, Kentuckyssa, Derbyshiressä, Etelä-Saksassa, Ranskan eteläosassa ja Venäjällä, ja fluorin tärkein lähde, (2) kryoliitti (Na 3 AlF 6)., pääasiassa Grönlannista, (3) fluoropaatiitti (Ca 5 [PO 4] 3 [F, Cl]), laajalle levinnyt ja sisältää vaihtelevia määriä fluoria ja klooria, (4) topaasi (Al 2 SiO 4 [F, OH] 2)), jalokivi ja (5) lepidoliitti, kiille sekä eläinten luiden ja hampaiden komponentti.