Joustavat ominaisuudet
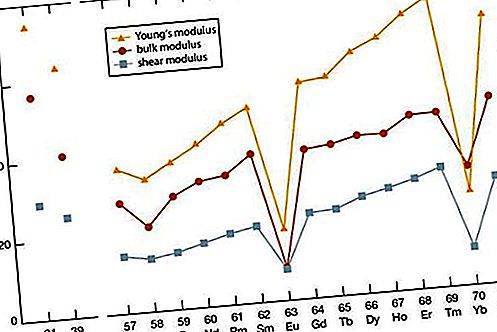
Kuten useimpien muiden harvinaisten maametallien ominaisuuksien kohdalla, myös harvinaisten maametallien elastiset moduulit kuuluvat muiden metalliosien keskipistepisteeseen. Skandiumin ja yttriumin arvot ovat suunnilleen samat kuin lantanidien pääteosien (erbium - lutetium) arvot. Elastinen moduuli lisääntyy yleisesti lisäämällä atominumeroa. Seerumin (noin 4f: n sitoutuminen) ja ytterbiumin (divalenssi) poikkeavat arvot ovat ilmeisiä.
Mekaaniset ominaisuudet
Harvinaiset maametallit eivät ole heikkoja eikä erityisen vahvoja metallielementtejä, ja niillä on kuitenkin vaatimaton taipuisuus. Koska mekaaniset ominaisuudet ovat melko voimakkaasti riippuvaisia metallien puhtaudesta ja niiden lämpöhistoriasta, on vaikeaa verrata kirjallisuudessa ilmoitettuja arvoja. Lopullinen lujuus vaihtelee välillä noin 120 - noin 160 MPa (megapaskalit) ja sitkeys noin 15 - 35 prosenttia. Ytterbiumin (europiumia ei ole mitattu) lujuus on paljon pienempi, 58 MPa, ja sitkeys on korkeampi, noin 45 prosenttia, kuten kaksiarvoiselle metallille voidaan odottaa.
Kemialliset ominaisuudet
Harvinaisten maametallien reaktiivisuus ilman kanssa osoittaa merkittävän eron kevyiden lantanidien ja raskaiden välillä. Kevyet lantanidit hapettuvat paljon nopeammin kuin raskaat lantanidit (gadoliini lutetiumin läpi), skandium ja yttrium. Tämä ero johtuu osittain muodostuneen oksidituotteen vaihtelusta. Kevyet lantanidit (lantaani neodyymin läpi) muodostavat kuusikulmaisen A-tyypin R 2 O 3 -rakenteen; keskellä lantanidit (samariumia kautta gadolinium) muodostavat monokliininen B-tyypin R 2 O 3 vaihe; kun taas raskas lantanideista, skandium ja yttrium, muodostavat kuutio C-tyypin R 2 O 3 muutos. A-tyyppi reagoi ilmassa olevan vesihöyryn kanssa muodostaen oksihydroksidia, joka aiheuttaa valkoisen päällysteen kaatumisen ja sallii hapettumisen tapahtua paljastamalla raikkaan metallin pinta. C-tyypin oksidi muodostaa tiiviin, yhtenäisen pinnoitteen, joka estää lisähapettumisen, samanlainen kuin alumiinin käyttäytyminen. Samarium ja gadolinium, jotka muodostavat B-tyypin R 2 O 3 -faasin, hapettuvat hiukan nopeammin kuin raskaammat lantanidit, skandium ja yttrium, mutta muodostavat silti yhtenäisen pinnoitteen, joka estää lisähapettumisen. Tämän vuoksi kevyitä lantanideja on varastoitava tyhjiössä tai inertin kaasun ilmakehässä, kun taas raskaat lantanidit, skandium ja yttrium voidaan jättää ulkona vuosiksi ilman hapettumista.
Europiummetallilla, jolla on bcc-rakenne, hapettuu nopeimmin kaikista harvinaisista maametalleista kostealla ilmalla, ja sitä on käsiteltävä jatkuvasti inertin kaasun ilmakehässä. Reaktiotuote europium, kun ne altistetaan kostea ilma on hydraatti hydroksidi, Eu (OH) 2 -H 2 O, joka on epätavallinen reaktiotuote, koska kaikki muut harvinaisten maametallien oksidin muodostamiseksi.
Metallit reagoivat voimakkaasti kaikki happojen paitsi vetyfluoridin (HF), vapauttaen H 2 kaasua ja muodostaa vastaavan harvinaisten maametallien-anionin yhdiste. Fluorivetyhappoon sijoitettuna harvinaiset maametallit muodostavat liukenemattoman RF 3- pinnoitteen, joka estää lisäreaktioita.
Harvinaisten maametallien helposti reagoida vetykaasun muodostamiseksi RH 2 ja samalla voimakkaasti hydridimuodostus- olosuhteissa RH 3 vaihe-lukuun ottamatta skandium, joka ei muodosta trihydride.
Yhdisteet
Harvinaisten maametallien elementit muodostavat kymmeniä tuhansia yhdisteitä, joissa kaikki alkuaineet ovat jaksollisen taulukon ryhmän 7 metallien (mangaani, teknetium ja renium) oikealla puolella ja beryllium ja magnesium, jotka sijaitsevat kaukana vasen puoli ryhmässä 2. Tärkeät yhdistelmäsarjat ja eräät yksittäiset yhdisteet, joilla on ainutlaatuiset ominaisuudet tai epätavallinen käyttäytyminen, kuvataan alla.
oksidit
Suurin tähän mennessä tutkittu epäorgaanisten harvinaisten maametallien yhdisteiden ryhmä on oksidit. Yleisin stökiometria on R 2 O 3 -koostumus, mutta koska harvoilla lantanidielementeillä on muita valenssitiloja 3+: n lisäksi, on olemassa muita stökiometrioita - esimerkiksi ceriumoksidi (CeO 2), praseodyymioksidi (Pr 6 O 11).), terbium oksidi (Tb 4 O 7), europiumoksidia (EuO), ja Eu 3 O 4. Suurin osa keskustelusta keskittyy binaarioksidiin, mutta myös kolmiosaisia ja muita korkeamman asteen oksideja tarkastellaan lyhyesti.