Happohappo, mikä tahansa happea sisältävä happo. Useimmat kovalenttiset ei-metalliset oksidit reagoivat veden kanssa muodostaen happamia oksideja; että on, ne reagoivat veden kanssa, jolloin muodostuu oksihapot että saanto hydronium-ioneja (H 3 O +) liuoksessa. On joitakin poikkeuksia, kuten hiilimonoksidia, CO, typpioksiduuli, N 2 O, ja typpioksidi, NO.
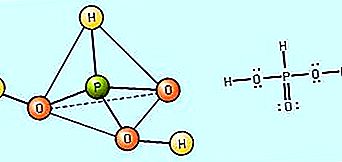
Oksihapon vahvuus määritetään sen mukaan, missä määrin se dissosioituu vedessä (ts. Sen kyky muodostaa H + -ioneja). Yleensä happohappojen suhteellinen lujuus voidaan ennustaa keskimääräisen ei-metallisen atomin elektronegatiivisuuden ja hapetuslukujen perusteella. Happolujuus kasvaa, kun keskusatomin elektronegatiivisuus kasvaa. Koska esimerkiksi kloorin (Cl) elektronegatiivisuus on suurempi kuin rikin (S), joka puolestaan on suurempi kuin fosforin (P), voidaan ennustaa, että perkloorihappo, HClO 4, on vahvempi happo kuin rikkihappoa, H 2 SO 4, jonka pitäisi olla vahvempi happo kuin fosforihappo, H 3 PO 4. Tietylle ei-metalliselle keskusatomille hapon voimakkuus kasvaa, kun keskusatomin hapetusluku kasvaa. Esimerkiksi typpihappo, HNO 3, jossa typpi (N) atomi on hapetusaste +5, on vahvempi happo kuin typpihapoke, HNO 2, jossa typen hapetusaste on +3. Samalla tavalla, rikkihappo, H 2 SO 4, rikin kanssa sen +6 hapetustilassa, on vahvempi happo kuin rikkihapoke, H 2 SO 3, jossa hapetustila on +4 määrä rikkiä on olemassa.
Oksihapon suola on yhdiste, joka muodostuu, kun happo reagoi emäksen kanssa: happo + emäs → suola + vesi. Tämän tyyppistä reaktiota kutsutaan neutraloimiseksi, koska liuos tehdään neutraaliksi.